|
Н.А. Галактионова
Промышленная экология
Учебное пособие для студентов заочного отделения / Москва: Международный независимый эколого-политологический университет, 2002
Тема 4. Основные технологические процессы
4.6. Массообменные процессы
Технологические процессы, скорость протекания которых определяется скоростью переноса вещества (массы) из
одной фазы в другую называются массообменными
процессами, а аппаратура, предназначенная
для проведения этих процессов, — массообменной аппаратурой.
Массообменные процессы занимают особое место
среди химико-технологических процессов.
В подавляющем большинстве
случаев производственные установки химической промышленности
создают по схеме, приведенной на рис. 4.26. Исходное сырье поступает в реактор, где
лишь частично превращается в продукты реакции. Выходящая из реактора смесь продуктов реакции и непрореагировавшего
сырья направляется в массообменную разделительную аппаратуру, в
которой производится разделение смеси на
продукты реакции и непрореагировавшее сырье.
Последнее возвращается в реактор, а продукты реакции поступают на дальнейшую переработку.
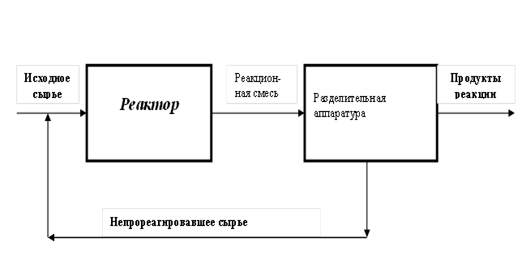
Рис. 4.26. Связь
реактора с разделительной аппаратурой
Из изложенного следует, что между реакционными и разделительными аппаратами существует тесная
технологическая связь. Общий закон этой связи таков: чем меньше
нагрузка на реакционный аппарат, т. е. чем меньше превращение исходного сырья в
продукты реакции, тем больше нагрузка на разделительный агрегат, и наоборот.
Очевидно, что оптимальное сочетание нагрузок на
реакционный и разделительный аппараты и приводит к минимальным производственным затратам — к оптимизированному процессу.
Следовательно, основа химического
производства — реакционный аппарат — работает оптимально только в сочетании с оптимально работающим
разделительным агрегатом и работа последнего имеет в химической промышленности
не меньшее значение, чем работа самого реакционного
аппарата.
В разделительном агрегате могут производиться
разнообразные процессы. Основными и важнейшими из них являются абсорбция,
экстракция, ректификация, адсорбция и сушка.
Абсорбция – избирательное поглощение
газов или паров жидкими поглотителями - абсорбентами. Процесс
используется во многих производствах, где из смеси газов необходимо извлечь
какой-либо компонент или группу компонентов. В этом процессе имеет место переход
вещества или группы веществ из газовой или паровой фаз в жидкую.
Экстракция [11] — извлечение
растворенного в одной жидкости вещества или группы веществ другой
жидкостью. Процесс используется в случаях, когда из раствора необходимо извлечь
растворенное вещество или группу веществ. В этом процессе имеет место переход
вещества из одной жидкой фазы в другую жидкую фазу.
Ректификация — разделение
жидкой смеси на чистые или обогащенные составляющие в результате противоточного
взаимодействия потоков пара и жидкости. Процесс имеет большое значение в тех производствах, где необходимо частичное или полное
разделение жидких однородных смесей на чистые компоненты или их группы. Очевидно, в этом процессе имеет место переход
вещества из жидкой фазы в
паровую, и наоборот.
Адсорбция — избирательное поглощение газов, паров или растворенных в жидкостях веществ твердым
поглотителем — адсорбентом, способным поглощать одно или несколько веществ
из их смеси. Процесс используется во
многих производствах, где из смеси газов, паров или растворенных веществ
необходимо извлечение того или другого
вещества. В этом процессе вещества переходят из газовой и жидкой фаз в твердую.
Сушка — удаление влаги из твердых
влажных материалов путем испарения. Процесс имеет большое значение во многих
производствах,
где влажные природные вещества до их переработки должны предварительно обезвожены или должен быть обезвожен готовый продукт, получающийся в последней
стадии производства. Нетрудно видеть, что в этом процессе имеет
место переход влаги из твердого влажного материала в паровую или газовую
фазу.
Из приведенной краткой характеристики следует, что для всех перечисленных процессов общим является
переход вещества из одной фазы в
другую, или массопередача. Переход вещества из одной фазы в
другую связан с явлениями конвективного переноса и молекулярной диффузии, поэтому перечисленные выше
процессы получили название массообменных
или диффузионных процессов. Массопередачей называют переход вещества
(или нескольких веществ) из одной
фазы в другую в направлении достижения равновесия.
В массообмене участвуют как
минимум три вещества: распределяющее вещество (или вещества),
составляющее первую фазу, распределяющее вещество (или
вещества), составляющее вторую фазу; распределяемое
вещество (или вещества), которое переходит из одной фазы
в другую (рис. 4.27).
Назовем первую фазу G, вторую L, а
распределяемое вещество M. Поскольку
все рассматриваемые массообменные процессы обратимы, распределяемое вещество
может переходить из фазы G в фазу L и наоборот, в зависимости от концентрации этого вещества в распределяющих фазах.
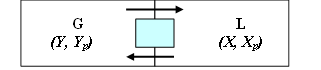
Рис. 4.27. Схема массобмена
G – распределяющее вещество 1-ой фазы; L -
распределяющее вещество 2-ой фазы;
М – распределяемое вещество; Х (Y) –
концентрация распределяемого вещества в фазе .L (G);
Xp (Yp) – равновесная концентрация распределяемого
вещества в фазе L (G)
Допустим, что распределяемое вещество
находится вначале только в фазе G и имеет концентрацию Y. В
фазе L в начальный момент
распределяемого вещества нет и, следовательно, концентрация его в этой фазе X = 0.
Если распределяющие фазы привести в
соприкосновение, начнется переход
распределяемого вещества из фазы G
в фазу L и в
последней обнаружится определенная
концентрация распределяемого вещества X > 0. С момента
появления вещества М в фазе L начинается и обратный переход его в
фазу G, но до некоторого момента число
частиц М, переходящих в единицу времени через единицу поверхности соприкосновения из фазы G в фазу L, больше, чем число
частиц, переходящих из фазы L в фазу G; конечным итогом процесса является переход М из фазы
G в фазу L.
Через определенный промежуток времени скорости перехода распределяемого
вещества из фазы G в
фазу L и обратно становятся одинаковыми. Такое состояние
называется равновесным. В состоянии равновесия
в каждом конкретном случае существует строго определенная зависимость между концентрациями
распределяемого вещества, которые
при равновесии системы называются равновесными, а достигнутые
концентрации – равновесными.
Очевидно, что любой концентрации X соответствует
равновесная концентрация Yp, и наоборот,
любой концентрации Y соответствует равновесная концентрация Хр,
т.е.
Хр, = f1(Y)
или Yp,
= f2(Х)
Приведенные выше функциональные зависимости
определяются в каждом случае особо, чему посвящен целый ряд специальной
литературы по процессам и аппаратам.
Знание равновесных концентраций
позволяет выяснить направление течения процесса, которое определяется
стремлением к равновесию. Если Y >. Yp, и, следовательно, X < Хр,
распределяемое вещество М будет переходить из фазы G в фазу L.
При условии Y <. Yp (X > Хр)
распределяемое вещество будет
переходить из фазы L в фазу G.
Так как
концентрация пропорциональна числу частиц, то, следовательно, скорость перехода распределяемого
вещества из одной фазы в
другую пропорциональна разности между фактической концентрацией распределяемого вещества в данной фазе
и равновесной концентрацией. Таким образом, движущей силой массообменных процессов являются разности
концентраций (Y – Yp) и (X – Xp).
4.6.1. Абсорбция
4.6.2. Ректификация
4.6.3. Экстракция
4.6.4. Адсорбция
4.6.5. Сушка
4.6.6. Кристаллизация
[11]
Имеется в
виду жидкостная экстракция.
|

