|
Н.В. Чибисова, Е.К. Долгань
Экологическая химия
Учебное пособие / Калинингр. ун-т. - Калининград, 1998. - 113 с.
7. Экологическая химия атмосферы
7.2. Фотодиссоциация
Солнце испускает энергию с разной длиной волны. Коротковолновое
излучение в ультрафиолетовой области спектра обладает высокой энергией,
вызывающей химические реакции. При этом энергия фотона (Е = hn) должна быть достаточна для разрыва химической
связи в молекуле и инициирования процесса. Кроме того, молекулы должны поглощать
фотон, энергия которого должна превращаться в какую-либо иную форму. Первая
реакция - фотодиссоциация кислорода:
О2 (г) + hn –> 2
О (г) . (1)
Максимальная энергия, которая
необходима для такого превращения, равна 495 кДж/моль. Можно выполнить
нетрудный расчет (см. ниже задачу) и определить, каковы должны быть n и l
этого излучения. l равна 242 нм.
Значит, любой фотон с длиной волны менее 242 нм имеет достаточную энергию для
этой реакции (чем короче l, тем выше
энергия).
Задача. Какая длина волны фотона
соответствует молярной энергии диссоциации связи 495 кДж/моль?
Решение. Сначала вычислим
энергию, необходимую для разрыва связи в одной молекуле.
Е` = 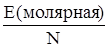 = = 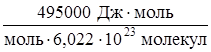 =
8,22·10–19 =
8,22·10–19 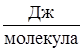 . .
Найдем частоту колебания, зная, что
энергия фотона Е = hn; n = 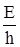 =
= =
= 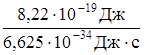 = 1,24·1015 с-1. = 1,24·1015 с-1.
Вспомним, что произведение частоты и
длины волны электромагнитного излучения равно скорости света: n·l =
с = 3,00·108 м/с; l =  = = = = 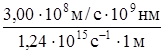 =
242 нм. =
242 нм.
К нашему счастью, молекулы О2
поглощают большую часть коротковолнового излучения с высокой энергией, прежде
чем оно достигнет нижней части атмосферы. При этом образуется атомарный
кислород. На высотах около 400 км диссоциировано 99% молекул кислорода, на долю
молекул О2 приходится лишь 1%. На высоте 130 км содержание О2 и О одинаково. На меньших высотах содержание молекулярного кислорода
больше такового атомарного.
Энергия диссоциации молекулы N2
очень велика, значит, разорвать молекулу могут только фотоны с чрезвычайно
высокой энергией и очень малой l. Таких
фотонов немного, да и молекула азота плохо поглощает фотоны, даже если их
энергия окажется достаточной. Вследствие этого атомарного азота очень мало.
Фотодиссоциация воды. Концентрация
паров воды значительна вблизи поверхности Земли, но быстро уменьшается с
высотой. На высоте 30 км (стратосфера) составляет три молекулы на миллион
молекул смеси. Однако, оказавшись в верхних слоях, вода подвергается
фотодиссоциации:
Н2О (г) + hn –> Н
(г) + ОН (г); (2)
ОН (г) + hn –> Н (г) + О
(г). (3)
Фотодиссоциация (уравнения 1-3)
осуществляется через процесс ионизации. В 1924 году было установлено, что в
верхних слоях атмосферы имеются свободные электроны, а по закону баланса
зарядов должны быть и положительно заряженные ионы. Откуда же берутся эти ионы?
В меньшей мере от воздействия электронов, прилетающих от Солнца вместе с
солнечным ветром, а в большей мере - вследствие фотодиссоциации. При воздействии
фотона молекула может поглотить его, не расщепляясь на атомы. При этом фотон
выбивает из молекулы электрон самого верхнего уровня, и образуется молекулярный
ион. Таким же образом может подвергнуться ионизации и нейтральный атом.
Фотоны, вызывающие ионизацию, относятся к
высокочастотной коротковолновой области в пределах ультрафиолета. Это излучение
не доходит до поверхности Земли, его поглощают верхние слои атмосферы (табл.
7.2).
Таблица 7.2
Реакции,
происходящие в верхних слоях атмосферы
|
Уравнение реакции
|
– DН ионизации кДж/моль
|
lmax, нм
|
|
N2 + hn –> N2+ + e
|
1495
|
80,1
|
|
O2 + hn –> O2+ + e
|
1205
|
99,3
|
|
O + hn –> O+ + e
|
1313
|
91,2
|
|
NO + hn –> NO+ + e
|
890
|
134,5
|
Необходимо обратить внимание на то, что все данные реакции экзотермические.
|

