|
В.Ф. Панин
Теоретические основы защиты окружающей среды
Конспект лекций по учебной дисциплине. Томск: ТПУ, 2009. – 115с.
2. Защита гидросферы от загрязнений
2.7. Очистка сточных вод
2.7.4. Физико-химические методы очистки сточных вод
Физико-химическая
очистка – один из наиболее распространённых методов очистки сточных вод. Этот
метод применяется самостоятельно или в сочетании с химическими, механическими,
биологическими методами [17-19].
2.7.4.1. Коагуляция, флокуляция и электрокоагуляция
В
практике очистки сточных вод метод коагуляции часто применяется после удаления
грубодисперсных примесей – для удаления коллоидных частиц. Коагуляция – процесс
слипания коллоидных частиц и образования грубодисперсной макрофазы (флокул) с
последующим её выделением из воды.
Один
из видов коагуляции – флокуляция, при которой мелкие взвешенные частицы под
влиянием специально добавляемых веществ (флокулянтов) образуют интенсивно
оседающие хлопьевидные образования.
Основной
процесс коагуляционной очистки сточных вод – гетерокоагуляция, при которой
коллоидные (и мелкодисперсные частицы) взаимодействуют с агрегатами,
образующимися при введении в стоки коагулянтов.
Основные
коагулянты: а) соли алюминия: глинозём Al2(SO4)3 ×18H2O; алюминат
натрия NaAlO2; оксихлорид
алюминия Al2(OH)5Cl; полихлорид
алюминия [Al2(OH)nCl6-n]m×(SO4)x,
где 1£ n £ 5m £ 10; б) соли железа: железный купорос FeSO4×7H2O; хлорид железа FeCl3×6H2O; сульфат железа Fe2(SO4)3×9H2; в) соли
магния: хлорид магния MgCl2×6H2O; сульфат
магния MgSO4×7H2O; г)
известь; д) шламовые отходы и отработанные растворы отдельных производств.
Сточные
воды смешивают с коагулянтом в специальных устройствах – смесителях в течение
1…3 мин., хлопьеобразование происходит в камерах хлопьеобразования, например, с
механическим перемешиванием. Осаждение хлопьев и частиц, образовавшихся в
результате коагуляции, производится в отстойниках, этот процесс часто называют
осветлением стоков, а соответствующие отстойники – осветлителями [18-20].
Согласно
современным представлениям [10], основная
масса коллоидных частиц имеет одинаковый отрицательный заряд и потому имеет
высокую агрегативную устойчивость. Появление в сточной воде положительных ионов
способствует нейтрализации электрических полей отрицательных зарядов коллоидных
частиц и они теряют свою агрегативную устойчивость. В наибольшей степени
агрегативную устойчивость частиц понижают ионы 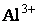 и и 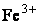 , и это обстоятельство предопределило
применение в качестве коагулянтов именно солей железа и алюминия. В последующем
практика и теория коагуляции привели к заключению, что в стоки достаточно
ввести не соли алюминия или железа, а только ионы , и это обстоятельство предопределило
применение в качестве коагулянтов именно солей железа и алюминия. В последующем
практика и теория коагуляции привели к заключению, что в стоки достаточно
ввести не соли алюминия или железа, а только ионы 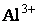 и и 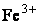 . Это достигается анодным растворением Al
или Fe в воде при прохождении через воду электрического тока. Такой процесс
коагуляции называется электрокоагуляцией, а соответствующие аппараты –
электрокоагуляторами. . Это достигается анодным растворением Al
или Fe в воде при прохождении через воду электрического тока. Такой процесс
коагуляции называется электрокоагуляцией, а соответствующие аппараты –
электрокоагуляторами.
2.7.4.2. Сорбция
Сорбция
– процесс поглощения вещества (сорбата) из очищаемой среды твёрдым телом или
жидкостью (сорбентом). Поглощение вещества массой жидкого сорбента – абсобция,
поверхностным слоем твёрдого сорбента – адсорбция. Если при поглощении
происходит химическое взаимодействие сорбента и сорбата, процесс называют
хемосорбцией.
При
очистке сточных вод в качестве сорбентов применяют искусственные и природные
пористые материалы: золу, коксовую мелочь, торф, силикагели, алюмогели,
активные глины. Наиболее эффективны активированные угли, пористость которых
достигает 75 %, а удельная площадь поверхности – 900 м2/кг. Расход
сорбента определяют из соотношения:
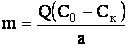 , ,
где
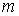 - масса сорбента, кг; Q – расход сточной
воды, м3/с; Co и Cк – концентрации примесей до
и после прохождения стоками сорбционной установки, кг/м3; а –
удельная активность сорбента – количество поглощаемого вещества на единицу
массы сорбента, кг/с. - масса сорбента, кг; Q – расход сточной
воды, м3/с; Co и Cк – концентрации примесей до
и после прохождения стоками сорбционной установки, кг/м3; а –
удельная активность сорбента – количество поглощаемого вещества на единицу
массы сорбента, кг/с.
На
рисунке 2.6 представлена схема сорбционной установки. Сточная вода поступает в
адсорбер 2 по трубопроводу 1. По трубопроводу 4 подаётся адсорбент,
перемешиваемый со стоками импеллером 3. Адсорбент с поглощёнными примесями оседает
на дно адсорбера, откуда удаляется через трубопровод 8. Сточная вода со
взвешенными частицами сорбента поступает в отстойник 5, в котором частицы
сорбента оседают на дно и удаляются по трубопроводу 7, а очищенная сточная вода
направляется по трубопроводу 6 для последующей обработки.
Обычно сорбционная установка представляет собой
несколько параллельно работающих секций, каждая из которых состоит из трёх-пяти
последовательно расположенных фильтров, схема которых представлена на рисунке
2.6.
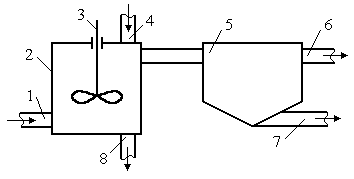
Рисунок 2.6 – Схема сорбционной установки
Регенерацию сорбентов производят экстрагированием
органическими растворителями; отгонкой водяным паром; испарением
адсорбированного вещества током инертного газообразного теплоносителя.
Вследствие обратимости процессов сорбции их целесообразно использовать для
очистки сточных вод от примесей, которые можно использовать повторно в
технологическом процессе.
2.7.4.3. Экстракция
Метод
применяется для удаления из стоков примесей, представляющих техническую
ценность (фенолы, жирные кислоты), основан на распределении примеси в смеси
двух взаимонерастворимых жидкостей (сточной воды и экстрагента) соответственно
коэффициенту экстракции (распределения) Кэ = Сэ/Св,
где Сэ и Св – концентрации примеси в экстрагенте и в
воде при установившемся равновесии. Так, для бутилацетата, который широко
используется для удаления из стоков фенола, коэффициент экстракции составляет
8...12. Экстрагент должен иметь следующие свойства: высокий Кэ;
селективность – способность экстрагировать из стоков одно вещество или
определённую их группу; малую растворимость в воде; плотность, отличающуюся от
плотности воды; нетоксичность; низкую стоимость и др.
Конечная
концентрация Св экстрагируемого вещества в стоках определяется из
соотношения:
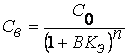 , ,
где
Со – начальная концентрация вещества в стоках, кг/м3; n –
число экстракций, В – удельный расход экстрагента для одной экстракции, м3/м3,
равный
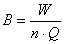  , ,
где
W – общий объём экстрагента, затрачиваемого на экстракцию, м3; Q –
объём стоков, подвергающихся экстракции, м3.
Регенерация
экстрагента из сточных вод и из экстракта (раствор примеси, удаляемой из
стоков, в экстрагенте) осуществляется водяным паром.
2.7.4.4. Ионный обмен
Метод
(гетерогенный ионный обмен или ионообменная сорбция) основан на процессе обмена
между ионами, находящимися в растворе (в сточных водах), и ионами,
присутствующими на поверхности твёрдой фазы – ионита. Молекулярная структура
ионита содержит матрицу – молекулу нерастворимого органического вещества – и
введенную в матрицу функциональную группу, способную обмениваться ионами с
очищаемым раствором. Наиболее распространены синтетические органические иониты
– ионообменные смолы. Иониты разделяются на катиониты и аниониты.
Катиониты
– материалы, способные обмениваться катионами, то есть положительными ионами.
Их функциональные группы, например, SO3H – сульфогруппа, СООН –
карбоксильная группа. При контакте с водой функциональная группа диссоциирует с
отщеплением иона водорода. Последний легко может быть вытеснен другим
положительным ионом, который, положим, необходимо удалить из сточной воды.
Реакция ионного обмена может быть записана в виде:
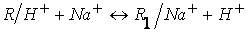 , ,
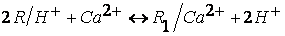 . .
Здесь
R обозначает комплекс катионитной матрицы и катионитной функциональной группы
без обменного иона (одновалентного), R1 – новый комплекс,
образовавшийся в результате объединения двух комплексов R двухвалентным ионом
кальция.
Значит, подобный ионообменный фильтр поглощает из
раствора ионы Na+, Ca2+ и т.д., а раствору передаёт ионы
водорода.
Аниониты
– материалы, способные обмениваться с раствором анионами, то есть
отрицательными ионами. По аналогии с катионитами, структура анионита может быть
обозначена как ROH, где R – комплекс анионитной матрицы и анионитной
функциональной группы.
Примеры
реакций обмена:
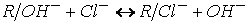 , ,
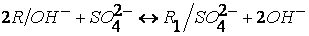 . .
Регенерация катионов производится слабыми растворами
кислот, например, 1,0…1,5 %-ным раствором серной кислоты:
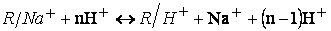 , ,
 . .
Регенерация анионитных фильтров производится обычно
4%-ным раствором NaOH.
Ионный
обмен производится в ионообменных фильтрах, которые в общих конструктивных
чертах подобны механическим зернистым насыпным фильтрам. При пропускании
сточной воды (прошедшей предочистку) через ионообменный фильтр частицы (зёрна)
ионитного фильтроматериала расходуют свой ионообменный ресурс, и фронт
насыщения ионами, удаляемыми из сточной воды, постепенно перемещается от входа
фильтра к его выходу. При «крутом» фронте насыщения имеет место наиболее полное
использование ионитного фильтроматериала. При подходе фронта насыщения к выходу
насыпного ионообменного фильтра подача сточной воды прекращается, чтобы не
допустить проскока через насыщенный фильтр ионов, удаляемых из сточной воды.
Насыщенный фильтр подлежит регенерации, а очищаемые сточные воды пропускаются
через свежий ионообменный фильтр.
2.7.4.5. Электродиализ
Этот
метод – вариант ионного обмена. Но в нём ионитный слой заменён специальными
ионообменными мембранами, а движущая сила – внешнее электрическое поле.
При
наложении постоянного электрического поля на раствор в последнем возникает
движение ионов растворённых солей, а также Н+ и ОН-. При
достижении катода катионы, а также молекулы воды восстанавливаются, например:
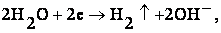
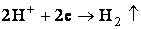 . .
На аноде происходит окисление анионов:
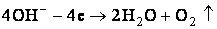 , ,
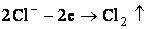 . .
Если в электродную ячейку поместить ионообменные
мембраны: катионообменную, пропускающую только катионы, - около катода, а около
анода – анионообменную, пропускающую только анионы, то объём ячейки разделится
на три камеры (рисунок 2.7). В этом случае в катодную камеру из средней могут
проходить лишь катионы, мигрирующие к катоду, а в анодную – анионы, мигрирующие
к аноду. Значит, концентрация ионов в средней (второй по счёту, чётной) камере
будет уменьшаться, в приэлектродных камерах – увеличиваться.
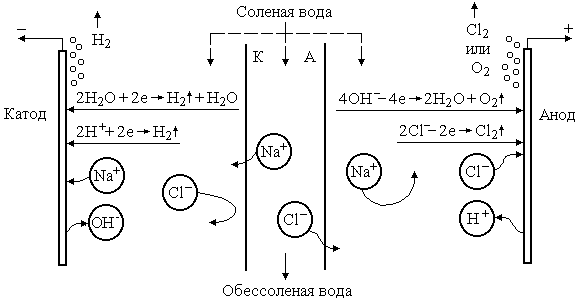
Рисунок 2.7 – Упрощенная принципиальная схема
электродиализатора
Если электродную ячейку разделить на множество камер,
то половина из них будет обессоливаться (чётные камеры), другая (нечётные
камеры) – наоборот, насыщаться. Значит, очищенной от солей является вода
(сточная вода) из чётных камер электродиализатора.
Мембраны
для аппаратов производят в виде гибких листов прямоугольной формы или рулонов
полимерного связующего с порошком ионообменных смол. Наиболее эффективное
использование электродиализаторов – при концентрации солей в сточной воде 3 ...
8 г/л.
2.7.4.6. Гиперфильтрация (обратный осмос) и
ультрафильтрация
Гиперфильтрация
– процесс непрерывного молекулярного разделения растворов путём их фильтрования
под давлением через полунепроницаемые мембраны, задерживающие полностью или
частично молекулы либо ионы растворённого вещества. При этом размеры отделяемых
частиц (молекул, гидратированных ионов) сопоставимы с размерами молекул
растворителя (воды). Необходимое давление, превышающее осмотическое давление
растворённого вещества в растворе, может достигать 5 ... 10 МПа.
Гиперфильтрация производится в случае относительно высокого осмотического
давления растворённого вещества в растворе.
В
растворах, содержащих высокомолекулярные вещества с максимальным диаметром
частиц 0,5 мкм, осмотическое давление пренебрежимо мало. Для их разделения
применяют процесс ультрафильтрации на специальных мембранах, пропускающих лишь
воду, ионы и молекулы низкомолекулярных соединений. В этом случае рабочее
давление в аппарате не превышает 0,5 МПа. Ультрафильтрацией также отделяют
коллоидные частицы и мелкодисперсные фракции грубодисперсных веществ.
Наибольшей
удельной площадью поверхности (на один кубический метр объёма аппарата, м2/м3)
обладают аппараты из полых волокон малого (45 ... 200 мкм) диаметра, 20000 м2/м3.
Производительность – до 1000 м3/сут.
2.7.4.7. Другие методы физико-химической очистки
сточных вод
Эвапорация.
Этот метод строится, в основном, либо на пароциркуляционном процессе, либо на
азеотропной ректификации. В первом случае загрязнения отгоняются с
циркулирующим водяным паром. При этом сточные воды движутся через колонку с
насадкой (загрузкой) навстречу острому пару, нагреваются до 100°С, при этом находящиеся в них летучие примеси переходят в паровую фазу.
Затем пар отмывается от загрязнений раствором щелочи.
Азеотропная
ректификация основана на свойстве ряда летучих соединений образовывать
нераздельнокипящие смеси с водой. В колоннах, обогреваемых паром, часть воды
отгоняется в виде азеотропной смеси с загрязняющим компонентом. Из нижней части
колонны выходят очищенные стоки, а из верхней части отводится пар и поступает в
конденсатор. Конденсат после охлаждения направляется на сепарацию, где
разделяется на два слоя - водный и органический. Водный слой сбрасывается в
ёмкость исходной сточной воды, загрязняющий компонент – на переработку или
использование.
Выпаривание.
Применяется для увеличения концентрации солей, содержащихся в сточных водах, и
ускорения их последующей кристаллизации, а также для обезвреживания небольших
количеств, например, радиоактивных сточных вод. Требует очень больших
энергетических затрат.
Испарение
осуществляется с открытой поверхности сточных вод на открытых испарительных
площадках, площадь которых рассчитывается в зависимости от климатических
условий и состояния грунтов.
Кристаллизация
основана на различной растворимости веществ, содержащихся в сточных водах, при
разных температурах. При изменении температуры получаются пересыщенные растворы
находящихся в них веществ, затем их кристаллы. Метод применяется при очистке
высококонцентрированных сточных вод.
Термоокислительные методы – парофазное окисление («огневой метод»), жидкофазное
окисление («мокрое сжигание»), парофазное каталитическое окисление.
При «огневом методе» сточные воды в распылённом
состоянии вводятся в высокотемпературные продукты горения топлива и испаряются,
при этом органические примеси сгорают. Минеральные примеси образуют твёрдые или
расплавленные частицы, они выводятся из рабочей камеры печи или уносятся с
дымовыми газами.
Жидкофазное окисление органических примесей сточной
воды кислородом воздуха производится при повышенных температурах (до 350°С) и давлении.
Термокаталитическое окисление. Сточные воды подаются в выпарной аппарат, где пары
воды и органических веществ, воздух и газы нагреваются до 300°С, затем смесь идёт в контактный аппарат, загруженный катализатором.
Обезвреженная смесь охлаждается, конденсат используется в производстве.
|

