|
Е.П. Гора
Экология человека
Учебное пособие для вузов. – М.: Дрофа, 2007. – 540 с.
Глава 3. Адаптация человека к экстремальным условиям среды
3.13. Действие ионизирующих излучений
Ионизирующие
излучения
– это
любые излучения, взаимодействие которых со средой приводит к образованию
электрических зарядов разных знаков, т. е. ионизации атомов и молекул в
облучаемом веществе. Кроме ионизации, все виды излучений вызывают возбуждение
атомов и молекул путем передачи им части энергии, недостаточной для ионизации.
Иначе говоря, ионизация и возбуждение являются главными процессами расходования
всей энергии излучения, проникающего в облучаемый объект. Ионизирующие
излучения подразделяются на электромагнитные и корпускулярные.
К электромагнитным
излучениям
относятся
рентгеновские лучи, гамма-лучи радиоактивных элементов и тормозное излучение,
испускаемое при изменении кинетической энергии заряженных частиц при
прохождении через вещество. Эти разновидности излучений имеют ту же природу,
что и видимый свет, радиоволны, но с меньшей длиной волны. Электромагнитные
излучения не имеют массы покоя и заряда, а потому обладают наибольшей
проникающей способностью. Пробег частиц электромагнитных излучений (фотонов)
максимально сокращается в таких материалах, как свинец, что используется при
конструировании защитных экранов.
Корпускулярное
излучение
– это
ионизирующее излучение, состоящее из частиц с массой покоя, отличной от нуля.
Выделяют две
разновидности подобных частиц. Заряженные частицы: β-частицы (электроны),
протоны (ядра водорода), дейтроны (ядра тяжелого водорода – дейтерия), α-частицы
(ядра гелия), тяжелые ионы – ядра других элементов, ускоренные до больших
энергий. При прохождении через вещество заряженная частица, теряя свою энергию,
вызывает ионизацию и возбуждение атомов. К незаряженным частицам относятся
нейтроны, которые не взаимодействуют с электронной оболочкой атома,
беспрепятственно проникают в глубь атомов, вступая в реакцию с ядрами. При этом
испускаются α-частицы или протоны. Протоны приобретают в среднем половину
кинетической энергии нейтронов и вызывают на своем пути ионизацию. Плотность
ионизации протонов велика, поэтому нейтроны следует рассматривать как частицы,
косвенно вызывающие очень плотную ионизацию. В веществах, содержащих много
атомов водорода (вода, парафин, графит), нейтроны быстро растрачивают свою энергию
и замедляются, что используется в целях радиационной защиты.
Основные источники
ионизирующих излучений. Различают два вида радиоактивности: естественную
(природную) и искусственную.
1. К естественным источникам излучений
относятся:
– внутренние: радиоактивные
изотопы
40К и 14С, отложившиеся в
костях радий и торий, а также радон, растворенный в тканях организма;
– внешние: космические лучи,
излучения от радиоактивности в почве, воздухе и строительных материалах.
Общая доза фонового
облучения, получаемая человеком в год, на уровне моря составляет примерно
0,14-0,7 сЗв. Учитывая, что современные самолеты летают на высотах более 10 км,
необходимо кратко охарактеризовать радиационную обстановку в верхних слоях
атмосферы и стратосфере. Основной вклад в дозу облучения на этих высотах вносит
галактическое космическое излучение (ГКИ). На уровне Земли доза от ГКИ
составляет 887 мкГр за год. Считается, что в пределах до 10 км над уровнем моря
доза ГКИ через каждые 1,5 км высоты удваивается. На высотах от 10 до 80 км она
изменяется в диапазоне от 1,8 до 8 сГр в год (или от 50 до 880 мкГр/сут.). На
высоте около 85 км над уровнем моря ГКИ формирует максимум тканевой дозы – до
8,64 сГр/год (840 мкГр/сут.). Этот максимум объясняется увеличением вклада
вторичного излучения (электроны, позитроны, протоны и др.). На высотах 85–30 км
вклад вторичного излучения уменьшается и интегральная доза составляет величину
порядка 5,4 сГр/год (150 мкГр/сут.).
2. Наиболее реальную
опасность представляют
искусственные источники излучений.
Совершенствование авиакосмической техники может привести к использованию в
будущем бортовых радиоизотопных, ядерно-энергетических и ядерно-силовых
установок, являющихся источниками ионизирующих излучений. Возникновение
радиационной ситуации возможно при перевозках радионуклидов, а также еще в трех
особых формах контакта с источниками облучения: взрыв ядерного оружия,
аварийный выброс технологических продуктов атомного предприятия в окружающую
среду и местное выпадение радиоактивных веществ, сопутствующее первым двум
обстоятельствам. Примерами могут служить атомный взрыв над городами Японии в
1945 году, испытательный термоядерный взрыв на Маршалловых островах в 1954
году, авария в Уайдскелле в 1957 году и др. Поток γ-излучения и нейтронов,
сопровождающий атомный взрыв, обладает значительной проникающей способностью и
достигает Земли даже при взрыве на значительной высоте.
Источником излучения
в районе взрыва являются также осевшие радиоактивные продукты из облака взрыва,
элементы почвы и местных предметов, приобретшие наведенную радиоактивность
вследствие воздействия потоков нейтронов из эпицентра взрыва.
Как естественная,
так и искусственная радиоактивность имеет сложный спектр излучения. Для оценки
биологического эффекта воздействия излучения произвольного состава введено
понятие эквивалентной дозы с единицей измерения в СИ – зиверт (Зв).
Зиверт – единица
эквивалентной дозы любого вида излучения в биологической ткани, которое создает
такой же биологический эффект, как и поглощенная доза в 1 Гр образцового
рентгеновского или г-излучения (энергия 100-1000 кэВ).
• При одной и той же
поглощенной дозе биологический эффект от воздействия различных видов излучения
существенно различается. В связи с этим для прогнозирования биологического
эффекта в поглощенную дозу излучения необходимо вносить поправочный коэффициент
на его вид: этот коэффициент характеризует относительную биологическую
эффективность (ОБЭ).
Пользуясь понятием о
дозе излучения, ОБЭ можно определить как отношение биологически равноэффективных
доз стандартного и сравниваемого излучений:

• Биологическую
эффективность ионизирующего излучения определяют в первую очередь линейной
плотностью ионизации (ЛПИ), создаваемой этим излучением, т. е. количеством пар
ионов, образуемых на единице пути ионизирующей частицы в веществе (ткани).
Однако биологическую эффективность правильнее связывать не с ЛПИ, а с величиной
энергии, передаваемой ионизирующей частицей ткани на единицу пути. Эта величина
называется линейной передачей энергии (ЛПЭ). Значения ЛПИ, ЛПЭ и ОБЭ связаны
между собой.
• Регламентированные
значения ОБЭ, установленные для контроля степени радиационной опасности в
области малых величин доз при хроническом облучении, называют коэффициентом
качества излучения Q.
• Кроме единиц дозы
излучения, в медицинской практике используют единицы активности радиоактивных
изотопов. Единица активности в СИ – беккерель (Бк), равная одному распаду в
секунду (расп./с).
Оценка дозы
осуществляется различными физическими и химическими методами. В настоящее время
широко используют ионизационный метод, т. е. измеряется электрический ток,
возникающий вследствие ионизации газовых смесей в специальных камерах с
тканеэквивалентными стенками. Важное значение для оценки облучения всего тела и
различных его частей имеют автономные дозиметры интегрального типа, в частности
термолюминесцентные дозиметры, достоинствами которых являются малые размеры,
устойчивость к механическим воздействиям и пониженному барометрическому
давлению, хорошая сохранность информации, химическая инертность, вследствие
чего возможно их употребление в любой газовой среде, при любой влажности.
Находит применение метод измерения дозы с использованием фотопленок и ядерных
фотоэмульсий. Применение ядерных фотоэмульсий позволяет, кроме того, проанализировать
состав падающего на тело излучения.
Биологическое
воздействие ионизирующих излучений. Первичные радиационно-химические изменения
при его воздействии раскрыты не полностью. В основе биовоздействия могут лежать
два механизма:
– прямое действие (молекула
биообъекта испытывает изменения непосредственно при прохождении через нее
электрона);
– косвенное (изменяемая молекула
получает энергию путем передачи от другой молекулы).
Все ткани организма
способны поглощать энергию излучения, которая преобразуется в энергию
химических реакций или тепло. Известно, что в тканях содержится 60–80 % воды.
Следовательно, большая часть энергии излучения поглощается водой, а меньшая –
растворенными в ней веществами.
Поэтому при
облучении в организме появляются свободные радикалы – продукты разложения
(радиолиза) воды, которые в химическом отношении очень активны, могут вступать
в реакцию с белковыми и другими молекулами. Полагают, что в таких «плотно
упакованных» структурах, как хромосомы, преобладают повреждения, обусловленные
прямым действием излучения, тогда как в растворах и высокогидратированных
системах существенную роль играют также продукты радиолиза воды.
При воздействии
очень больших доз в результате первичного действия ионизирующего излучения
наблюдаются изменения в любых биомолекулах. При умеренных же дозах лучевого
воздействия первично страдают в основном только высокомолекулярные органические
соединения: нуклеиновые кислоты, белки, липопротеиды и полимерные соединения
углеводов.
• Нуклеиновые
кислоты обладают чрезвычайно высокой радиочувствительностью. При прямом
попадании достаточно 1–3 актов ионизации, чтобы молекула ДНК вследствие разрыва
водородных связей распалась на две части и утратила свою биологическую
активность.
• При воздействии
ионизирующего излучения в белках происходят структурные изменения, приводящие к
потере ферментативной и иммунной активности. Нарушение структуры белков
проявляется в изменении ряда их физических характеристик: показателях вязкости,
преломления света, оптического вращения, спектрах электронного парамагнитного
резонанса и др. Обнаружение свободных амидных групп и фрагментов после
раскручивания молекул облученных белков свидетельствует о наличии
замаскированных разрывов полипептидных цепей. С увеличением дозы излучения
число разрывов полипептидных связей нарастает и явления деградации белка
становятся очевидными.
• Повреждение
ионизирующим излучением структуры жиров приводит к нарушению сложных
ферментативных реакций, развитие которых обеспечивается упорядоченностью
расположения ферментов на мембране, а также изменению процессов адсорбции и
активного транспорта ряда веществ через мембрану вследствие нарушения ее
проницаемости. Первичные изменения в жирах при воздействии ионизирующего
излучения заключаются в образовании свободных радикалов, которые,
взаимодействуя с кислородом, образуют перекисные соединения, обладающие высокой
химической активностью.
Первичные изменения
в углеводах сводятся к окислению их с распадом углеводородной цепи и
образованием кислот и формальдегида.
В результате этих
процессов, протекающих практически мгновенно, образуются новые химические
соединения – радиотоксины, несвойственные организму в норме. Все это приводит к
нарушению сложных биохимических процессов обмена веществ и жизнедеятельности
клеток и тканей, т. е. к развитию лучевой болезни (рис. 3.6).
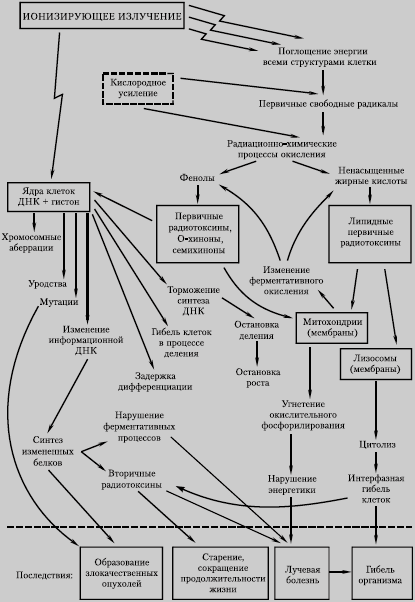
Рис. 3.6. Механизмы
развития радиационного поражения (по: А. М. Кузин, 1970)
Проблема
радиочувствительности клеток, тканей, организмов занимает центральное место в
радиобиологии. Наиболее чувствительны к этому фактору малодифференцированные,
молодые и растущие клетки. Характеристикой радиочувствительности биообъектов
является величина дозы облучения, вызывающей гибель 50 % объектов. У человека
среднелетальная доза равна 4 ± 1 Гр.
Формы лучевой
болезни. Ввиду
различной радиочувствительности органов и тканевых систем существует строгая
зависимость между поглощенной дозой в организме и средней продолжительностью
жизни биологических объектов. Эти три характерных дозных участка кривой,
отражают основные клинические радиационные синдромы (формы лучевой болезни),
развивающиеся вследствие необратимого поражения соответствующих критических
систем (органов) организма: кроветворной, кишечника и ЦНС:
– костномозговой
(1-10 Гр);
– желудочно-кишечный
(10–50 Гр);
– церебральный
(более 50 Гр).
Критический орган (система) – это система,
орган, ткань или часть тела, которая первой выходит из строя в конкретном
диапазоне доз и приводит организм к гибели, а в гигиеническом плане причиняет
наибольший ущерб здоровью человека или его потомству.
• Костномозговая
форма лучевого поражения возникает в результате однократного, общего
относительно равномерного облучения, когда критической является система
кроветворения и в первую очередь костный мозг. Эта форма клинически может протекать
в виде:
– острой лучевой
реакции;
– острой лучевой
болезни.
Острая лучевая
реакция
Наиболее легкая
степень тяжести острого лучевого поражения организма. Она наблюдается при
небольших дозах облучения (порядка нескольких десятых долей грэй). Самочувствие
остается удовлетворительным; какие-либо выраженные клинические проявления у
пораженных отсутствуют. При исследовании крови находят умеренно выраженное
уменьшение содержания лимфоцитов, гранулоцитов и тромбоцитов. Изменения в целом
носят преходящий характер и через 3–4 недели исчезают. Смертельные исходы
отсутствуют.
Острая лучевая
болезнь (ОЛБ)
Это более тяжелое
поражение организма. Оно возникает при относительно больших дозах облучения –
порядка нескольких грэй. Характерной чертой ОЛБ является волнообразностъ клинического
течения.
Предлагается
различать три периода в течении ОЛБ: формирование, восстановление и период
исходов и последствий.
I. Период формирования
ОЛБ, в свою очередь, четко разделяется на четыре фазы.
1. Фаза первичной
общей реакции
–
наиболее ранний симптомо-комплекс радиационного поражения, возникающий в первые
часы после облучения и характеризующийся следующими симптомами: общая слабость,
утомляемость, апатия, головокружение, головная боль, парестезии конечностей,
нарушение сна, тошнота, рвота, понос. Ясно, что в условиях полета указанные
симптомы могут приобрести особую значимость. Бесспорно, перечисленные симптомы
являются «поведенчески значимыми». Однако заранее невозможно однозначно
прогнозировать, какое влияние окажут соматические и психосоматические эффекты
облучения на операторскую деятельность, поскольку высокий уровень тренировки и
мотивации позволяет выполнять сложные задачи управления в различных
экстремальных условиях.
2. Фаза кажущегося
клинического благополучия (скрытая, или латентная). Чем короче срок
такого состояния, тем, как правило, тяжелее степень радиационного поражения.
Несмотря на отсутствие видимых клинических проявлений, отмечаются
функциональные нарушения в ЦНС, а также в сердечно-сосудистой, кроветворной и
пищеварительной системах. Непродолжительный абсолютный нейтрофильный лейкоцитоз
сменяется лейкопенией со сдвигом формулы вправо. С первых минут или часов после
облучения обнаруживается лимфоцитопения, быстро снижается число нейтрофилов,
затем тромбоцитов и позже эритроцитов. Продолжительный начальный лейкоцитоз
(2–3 дня после облучения) является, как правило, благоприятным прогностическим
признаком.
3. Фаза выраженных
клинических проявлений
(разгар
заболевания) характеризуется появлением всего симптомокомплекса лучевой
болезни.
4. Фаза
непосредственного восстановления, переходящая в период восстановления.
II. Процессы
восстановления в облученном организме характеризуются периодом
полувосстановления, т. е.
временем, необходимым для восстановления организма от лучевого поражения на 50 %.
У человека, согласно расчетам, он составляет 25–45 дней, считая от момента
облучения. В среднем его принимают равным 28 суткам.
Восстановление
происходит не во всех случаях облучения. Предлагается различать 4
прогностические категории:
1) выживание
невозможно, если доза облучения основной массы тканей тела достигает 6 Гр,
несмотря на отличный медицинский уход и самую современную терапию;
2) выживание
возможно при дозах 2–4,5 Гр, несмотря на тяжелое поражение, которое требует своевременного
и квалифицированного лечения;
3) выживание вполне
вероятно (1–2 Гр);
4) выживание
несомненно (при дозах менее 1 Гр), а имеющаяся клиническая симптоматика (только
гематологические сдвиги) не требует медицинского вмешательства.
III. Период исходов и
последствий облучения проявляется в изменениях крови, угнетении механизмов
иммунитета, нарушении обмена веществ, а далее – укорочении продолжительности
жизни (раннее старение), увеличении вероятности развития лейкоза и
злокачественных новообразований, помутнения хрусталика (лучевая катаракта),
нарушении функции сердечно-сосудистой системы, вегетативных расстройствах, а
также в генетических изменениях.
• При кишечной форме лучевой болезни в
результате массовой гибели клеток эпителия тонкого кишечника развиваются
тяжелые нарушения в желудочно-кишечном тракте. Резко нарушаются процессы
всасывания и экскреции веществ. Организм теряет много жидкости, наступает его
обезвоживание. Слизистая оболочка изъязвляется, иногда появляются перфорации,
развиваются кишечные кровотечения, являющиеся нередко причиной смерти
пораженных. Большую роль играют при этой форме поражения также инфекция и
интоксикация организма продуктами жизнедеятельности кишечной микрофлоры.
Глубокие патологические изменения в кроветворной ткани не успевают развиться,
так как пораженные умирают в ближайшие 6–9 дней после облучения. Однако,
несмотря на быстротечность заболевания, и в этом случае можно отметить короткий
период мнимого благополучия, длящийся от 1 до 2 суток.
• Церебральная
форма
лучевого
поражения характеризуется чрезвычайно быстрым и тяжелым течением.
Продолжительность жизни пораженного измеряется часами. Уже вскоре после
облучения появляются мышечный тремор, нистагм, расстройство равновесия и
координации движений, тонические и клонические судороги. Развивается состояние
децеребрационной ригидности мышц. Во время приступа останавливается дыхание.
Может наступить паралич дыхательного центра. Кишечная и церебральная формы
лучевой болезни клинически протекают в виде острейшей лучевой болезни.
Описанные
биологические эффекты могут значительно модифицироваться условиями облучения:
время, локализация, сопутствующие факторы. Так, например, большое значение
имеет мощность дозы, или интенсивность облучения, под которой понимают
количество энергии излучения, поглощаемое в единицу времени – сутки, час,
минуту, секунду и т. д. Если мощность дозы очень мала, то даже ежедневные
облучения в течение всей жизни человека не смогут оказать заметно выраженного
поражающего действия. Таким образом, фактор времени крайне значим в
биологическом эффекте излучения. Это еще раз свидетельствует о том, что
организм обладает способностью восстанавливать основную часть радиационного
поражения. Многократное прерывистое (фракционированное) воздействие излучения также
приводит к значительному снижению поражающего действия. Неравномерные лучевые
воздействия, которые встречаются на практике в подавляющем большинстве случаев,
переносятся в целом значительно легче, чем «классические» общие равномерные
облучения, рассмотренные нами ранее.
Таким образом, в
настоящее время достаточно хорошо изучены последствия, вызываемые воздействием
на организм различного рода ионизирующих излучений. Однако физиологические
реакции, возникающие под их влиянием, в сочетании с другими факторами нелучевой
природы могут быть существенно иными.
Лечение и
профилактика радиационного облучения. В настоящее время разработаны эффективные
меры и правила защиты людей, работающих с источниками ионизирующих излучений.
Профилактика радиационных поражений осуществляется путем проведения комплекса
санитарно-гигиенических, санитарно-технических и специальных медицинских
мероприятий.
Строгое соблюдение
правил и надлежащий дозиметрический контроль исключают вредное действие
ионизирующих излучений.
I. Средства противохимической
защиты
(защитная
одежда, противогазы или респираторы и т. п.) оказывают известный защитный
эффект от воздействия радиоактивных веществ. Эффективным способом
противорадиационной защиты является локальное экранирование критических органов
и систем. В случаях, когда неизбежно облучение в дозах, превышающих предельно
допустимую дозу (ПДД), профилактика осуществляется методом фармакохимической
защиты.
При попадании
радиоактивных веществ на открытые участки тела, одежду, снаряжение основная
задача сводится к быстрому их удалению, чтобы воспрепятствовать попаданию
радионуклидов в организм. Если радиоактивное вещество все же проникло внутрь,
то пострадавшему сразу вводят адсорбенты в желудок (промывают его, дают
рвотные, слабительные, отхаркивающие средства) и внутривенно – комплексионы
(например, динатриевая соль этилендиамино-тетрауксусной кислоты – ЭДТУ),
способные прочно связывать радиоактивные вещества и препятствовать отложению их
в тканях.
Основным требованием
при лечении ОЛБ является комплексность терапевтических мероприятий, при этом
используют как патогенетические, так и симптоматические средства.
II. Радиопротекторы. В результате
многочисленных радиобиологических исследований обнаружены вещества, которые при
введении в организм за определенное время до облучения снижают в той или иной
степени радиационное поражение. Большинство изученных в настоящее время
радиопротекторов оказывают положительный эффект при введении их в организм за
сравнительно короткое время до облучения. Они улучшают течение лучевой болезни,
ускоряют восстановительные процессы, повышают эффективность терапии и
увеличивают выживаемость.
Одним из основных механизмов модификации
радиочувствительности, в том числе и при использовании радиопротекторов,
является кислородный
эффект –
универсальное явление радиобиологии. Под ним обычно понимают явление усиления
лучевого поражения при повышении концентрации кислорода в облучаемой среде во
время облучения и, напротив, ослабление поражения при снижении его концентрации
в биологическом объекте. Кислородный эффект продемонстрирован на молекулярном,
клеточном, тканевом и организменном уровнях биологической интеграции.
Применение кислорода после момента облучения может привести к качественно иным
изменениям, в частности возможно улучшение и убыстрение восстановительных
процессов.
Таким образом, было
экспериментально установлено, что повышения радиорезистентности организма можно
добиться, применяя фармакохимические средства (в том числе и дыхание
гипоксическими газовыми смесями), которые способны тем или иным способом
вызывать гипоксию в клетках и тканях облучаемого организма.
• Механизмы
защитного действия радиопротекторов:
– конкуренция за
сильные окислители и свободные радикалы, образовавшиеся в результате радиолиза
воды;
– увеличение содержания
в тканях эндогенных тиоловых соединений;
– образование
временных, обратимых связей с чувствительными группами жизненно важных
ферментов или другими белковыми молекулами, предохраняющее их от повреждающего
действия в момент облучения;
– торможение цепных
реакций окисления с разветвленными цепями, связывающими активные радикалы и
вызывающими обрыв реакции;
– образование
прочных соединений с тяжелыми металлами, обеспечивающими ускоренное течение
этих реакций;
– миграция избытка
энергии с макромолекулы на радиопротектор;
– поглощение
вторичного ультрафиолетового излучения, возбуждающего макромолекулы типа
нуклеиновых кислот;
– замена составных
частей жизненно важных молекул;
– повышение
устойчивости и мобильности защитных механизмов организма;
– детоксицирование
или ускоренное выведение из облученного организма токсических продуктов;
– снижение уровня
обмена веществ;
– предупреждение
нарушения взаимодействия процессов возбуждения и торможения в ЦНС.
• Работы по созданию
радиозащитных препаратов проводятся по двум путям.
1. Первый путь
предусматривает
улучшение
переносимости радиопротекторов
с помощью физиологически активных веществ (витамины, стимуляторы ЦНС и т. д.),
предотвращающих или ослабляющих побочные эффекты.
2. Второй путь основан
на использовании особенностей механизма действия радиопротекторов различного
вида. В комплекс включают препараты, противолучевое действие которых при их
совместном применении
суммируется или потенцируется.
III. Биологическая
защита.
Кроме
радиопротекторов, должное внимание следует уделять биологической защите,
которая осуществляется с помощью адаптогенов. Эти вещества не обладают
специфическим действием, но зато повышают общую сопротивляемость организма к
различным неблагоприятным факторам, в том числе и к ионизирующим излучениям.
Адаптогены назначают многократно за несколько дней или недель до облучения. К
ним следует отнести препараты элеутерококка, женьшеня, лимонника китайского,
витаминно-аминокислотные комплексы, некоторые микроэлементы, АТФ, дибазол,
гутимин и др. Механизм действия этих препаратов необычайно широк. Так,
например, они увеличивают способность кроветворных клеток к пролиферации,
повышают иммунологическую реактивность и т. п. В понятие биологической защиты
входят и такие мероприятия, как акклиматизация к гипоксии, вакцинация, хорошее
питание, занятия физической культурой и т. д. Все это, безусловно, повышает
устойчивость организма. Напротив, злоупотребление алкоголем, никотином,
наркотиками снижает устойчивость организма к облучению.
|

