|
А.Н. Петин, М.Г. Лебедева, О.В. Крымская
Анализ и оценка качества поверхностных вод
Учебное пособие. – Белгород: Изд-во БелГУ, 2006. – 252 с.
1. Водоемы и показатели качества воды
1.3. Растворенный в воде кислород
1.3.3. Бихроматная окисляемость (ускоренный метод определения)
Определение бихроматной окисляемости может
проводиться арбитражным и ускоренным методами. Оба метода
являются титриметрическими. Ввиду сложности арбитражного метода
определения ХПК ниже мы приводим только ускоренный метод, который
можно считать упрощенной модификацией арбитражного. Приводимый метод
вполне может быть реализован в полевых условиях или при отсутствии
лабораторной базы (например, в производственных условиях) и пригоден
для анализа сточных и загрязненных природных вод. Он нашел
применение для постоянных ежедневных анализов, проводимых для контроля работы
очистных сооружений, состояния воды в водоемах и др.
Результаты определений, получаемые ускоренным методом, обычно
несколько ниже, чем при анализах арбитражным методом, однако они
хорошо воспроизводимы и коррелируют с его результатами. Воспроизводимость
результатов, получаемых ускоренным методом, объясняется тем, что в одном
и том же водоеме (сточной воде, технологической пробе и
т.п.) присутствует практически один и тот же «букет» окисляемых
органических соединений. Расхождения между результатами
ускоренного и арбитражного методов могут быть значительными в
тех случаях, когда в пробах присутствуют трудно окисляемые вещества – например,
уксусная кислота,
аланин, бензол и др. Практически же вводят коэффициент пересчета для корректировки результатов ускоренного метода и их приведения (с некоторой погрешностью) к
арбитражному.
Главная особенность ускоренного метода
определения ХПК – повышенная концентрация используемого раствора серной кислоты (применяется
неразбавленная концентрированная серная кислота). В таких условиях не требуется
специального нагревания пробы, т.к. ее
температура повышается до необходимых
значений за счет тепла, выделяемого при разбавлении серной кислоты. Именно в этом состоит основное отличие
ускоренного метода от арбитражного,
т.к. в последнем пробу необходимо кипятить
более часа в сернокислотном растворе бихромата калия. Это создает ряд
преимуществ ускоренного метода перед арбитражным, расширяет область его применения. Следует отметить, что при
определении ХПК ускоренным методом окисление проводят без добавления катализатора – сульфата серебра. При этом несколько снижается точность анализа за счет
неполного окисления части трудно
окисляющихся органических веществ.
Ускоренный метод применяется при значениях ХПК не менее
50 мгО/л и не более 4000 мгО/л, при больших значениях пробу необходимо
разбавить.
Оборудование и реактивы
Колба коническая плоскодонная из термостойкого стекла на
150-200 мл, пипетка-капельница, пипетки
мерные, цилиндр мерный
на 100 мл.
Защитные очки, перчатки.
Вода дистиллированная или бидистиллированная,
раствор бихромата калия (0,25 н.), раствор соли Мора
титрованный, серная кислота концентрированная, сульфат ртути (II) кристаллический в капсулах по 0,2 г, раствор индикатора ферроина.
Примечание. Воду
дистиллированную необходимо проверить на отсутствие органических
веществ в холостой пробе.
О приготовлении растворов см. приложение 3.
Отбор и хранение
проб
Количество пробы,
отбираемой на анализ ускоренным методом, зависит от ожидаемого значения ХПК
исследуемой воды. Соответствующие данные приведены в табл. 20.
Таблица 20
|
Ожидаемое значение
ХПК
|
Количество пробы
для анализа
|
|
50-500
|
5 мл
|
|
500-4000
|
1 мл
|
|
Свыше 4000
|
Пробу необходимо разбавить
|
В зависимости от
целей анализа определение ХПК можно проводить в нефильтрованной или фильтрованной
пробе. В последнем случае пробу фильтруют через мембранный или бумажный фильтр.
Определение ХПК
1. В коническую колбу
на 150-200 мл с помощью пипетки поместите пробу воды в необходимом количестве (см. табл. 20).
2. К пробе пипеткой добавьте 2,5 мл 0,25 н. раствора
бихромата
калия.
3. К раствору добавьте содержимое капсулы (около 0,2 г) сульфата ртути (II).
4. К содержимому колбы, перемешивая
раствор покачиванием, осторожно добавьте пипеткой концентрированную серную
кислоту в количестве 7,5 мл на 1 мл пробы либо 15 мл на 5 мл пробы (техника
безопасности!)
Примечание. В данной операции
температура раствора поднимается выше 100 ºС.
5.Колбу выдержите 2
мин., после чего раствор охладите до комнатной температуры.
6. В колбу мерным
цилиндром прилейте 100 мл дистиллированной воды.
7. В колбу добавьте 3-4
капли раствора ферроина.
8.Оттитруйте избыток
бихромата раствором соли Мора с помощью пипетки или бюретки.
При титровании
определите объемы раствора соли Мора, расходуемые в ходе анализа (VА = VАО – VАК), и в холостом
опыте (Vх = Vхо – Vхк).
9. Проведите
холостой опыт, используя вместо пробы
чистую дистиллированную или бидистиллированную воду в том же количестве.
По результатам
титрования вычисляется ХПК исследуемой пробы воды по следующей формуле:
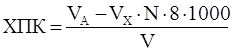
где VА и Vх – объемы раствора
соли Мора, израсходованного на титрование в холостом опыте и при анализе пробы
соответственно,
мл;
N – нормальность титрованного раствора
соли Мора, г-экв/л;
V – объем анализируемой пробы сточной воды, мл;
8 – эквивалент
кислорода.
Контроль точности анализа
Контроль точности
анализа на бихроматную окисляемость проводят с помощью стандартного раствора, в
качестве которого используют водный раствор бифталата калия (КС8Н5О4)
в концентрации
2,0824 ммоль/л. Потребление кислорода при использовании такого раствора в качестве
пробы соответствует значению ХПК 500 мгО/л.
|

