|
Е.А. Зилов
Гидробиология и водная экология
Учебное пособие. – Иркутск: Иркут. ун-т, 2007.
Раздел 2. Организация водных экосистем
6. Разнообразие и классификации озер
6.1. Гидросфера
Водная оболочка составляет 0,025 % (0,25·10–3)
массы Земли. Объем гидросферы 1375·106 км3. Океаны
покрывают 70,8 % земной поверхности и имеют среднюю глубину 3,96 км. В
каждом кубическом километре морской воды растворено 36 миллионов тонн твердых
веществ. Средний химический состав растворенных в морской воде веществ: Cl –
55,07 %, Na – 30,62 %, Mg – 3,68 %, S – 2,73 %, Ca –
1,18 %, K – 1,10 %, Br – 0,19 %, C – 0,08 %, Sr –
0,02 %, B – 0,01 %. Средний ионный состав океанской и пресной воды
дан в таблице 2, состав озерных и речных вод – в таблицах 3 и 4.
Вода (H2O) – одно из самых замечательных веществ.
Она - самое привычное для нас химическое соединение. Мы пьем воду, готовим пищу
на воде, умываемся водой, стираем в воде, плаваем в воде. На 2/3 мы состоим из
воды, и не можем без нее жить. Жизнь, как известно, развилась в воде и
немыслима без воды. Вода часто причиняет нам неприятности: отсутствие ее –
засухи, избыток – наводнения и потопы. Благодаря своей важности вода кажется
одним из самых исследованных веществ на Земле, но неожиданно оказалось, что
вода полна загадок не только для обывателей, но и для ученых, постоянно ее
исследующих.
С первого взгляда вода кажется очень простым химическим
соединением, молекула которого состоит из двух атомов водорода, присоединенных
к атому кислорода. В самом деле, мало найдется молекул, меньших, чем молекула
воды. Тем не менее, размеры молекул скрывают всю необыкновенную сложность их
свойств, а ведь именно эти свойства идеально соответствуют требованиям жизни,
или даже наоборот – создают условия самого существования жизни.
На поверхности планеты существует только две неорганические жидкости
– вода и металлическая ртуть. Все ближайшие «родственники» воды: аммиак,
сероводород, метан – газы. В газообразном состоянии при нормальных условиях
должна находиться и вода.
При 0 °С каждая молекула жидкой воды совершает 1011 – 1012
движений в секунду, каждая молекула льда – 105 – 106.
Вода расширяется при замерзании, т.ч. образовавшийся лед занимает объем,
больший, чем исходная жидкая вода. Это объясняется тем, что молекулы жидкой
воды двигаются свободнее и поэтому могут располагаться компактнее. Именно
поэтому лед плавает на поверхности воды, в отличие от большинства других
веществ для которых характерна большая плотность твердой фазы по сравнению с
жидкой. Если бы и вода вела себя таким же образом, то лед погружался бы на дно
водоема, а не защищал бы жидкую воду от дальнейшего охлаждения и
кристаллизации. В результате бы наша планета была покрыта сплошной ледяной
коркой и жизнь была бы невозможна.
Плотность воды возрастает с ростом температуры от 0 °С до 3,98 °С. По превышении температуры 4 °С движения молекул воды становятся
интенсивнее и плотность воды начинает снижаться
Удельная теплоемкость воды также аномально высока. Для того,
чтобы поднять температуру 1 г воды на 1 °С мы должны затратить 4,186 кДж тепла. Для сравнения
можно указать, что для такого же разогрева льда нам потребуется 2,04 кДж, а
воздуха – 1,00 кДж. Лишь немногие вещества характеризуются теплоемкостью,
сопоставимой с теплоемкостью воды (жидкий литий, жидкий водород, жидкий
аммиак).
Высокая теплоемкость превращает водоемы в аккумуляторы
тепловой энергии, влияющие на климат. Так, с поверхности озера, расположенного
на 50 ° широты с мая
по октябрь испаряется до 60 см воды, что эквивалентно потере половины
приходящей на поверхность водного зеркала солнечной энергии. В условиях тропиков
практически вся приходящая на поверхность озера солнечная энергия уходит на
процессы испарения. Таяние 1 м3 льда также предотвращает нагревание
10 м3 воды.
Скорость изменения плотности воды с температурой выше при
высоких температурах. Это неизбежно воздействует на процессы перемешивания воды
– чем выше температура воды, тем больше энергии требуется на ее перемешивание.
Важными параметрами являются поверхностное натяжение и вязкость.
Сила поверхностного натяжения воды достаточно велика и составляет 7,3×10-3 Н м-1.
Выше поверхностное натяжение только у жидкой ртути. Поверхностное натяжение
уменьшается с ростом температуры, в присутствии поверхностно-активных веществ,
включая гуминовые вещества и продукты выделения водорослей.
Вязкость воды также уменьшается с температурой. Чем выше
вязкость жидкости, тем легче организмам «парить» в такой жидкости, чем ниже
вязкость – тем легче осуществлять активное плавание.
Вода чрезвычайно плохо сжимаема, характеризуется низким
коэффициентом теплового расширения.
Чем же можно объяснить аномальные свойства воды? В настоящее
время их объясняют молекулярной структурой воды, наличием водородных связей и
поведением воды как «жидкокристаллического» тела (Chaplin, 2002).
Подавляющая часть воды на Земле сосредоточена в Мировом Океане.
Если гипотетически распределить всю воду планеты на поверхности шара с площадью
равной земной, то мы получим слой воды мощностью 2,6 км. Толина слоя пресной
воды при этом составила бы 50 м. Из них 49,5 м – вода,
сосредоточенная в полярных льдах и ледниках и только 0,5 м – вода,
находящаяся в озерах и водохранилищах, т. е., доступная для использования
человечеством. Наглядно это представлено на рисунке 7. Поскольку именно пресные
водоемы особенно важны для человечества как производители и хранилища доступной
питьевой воды, в дальнейшем изложении мы сосредоточимся именно на пресных
водах.
Таблица 2
Средний ионный состав (в %) морской и
пресной воды
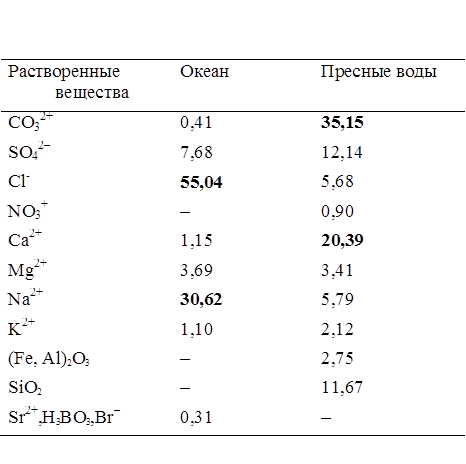
Таблица 3
Средний состав (в %) озерных вод

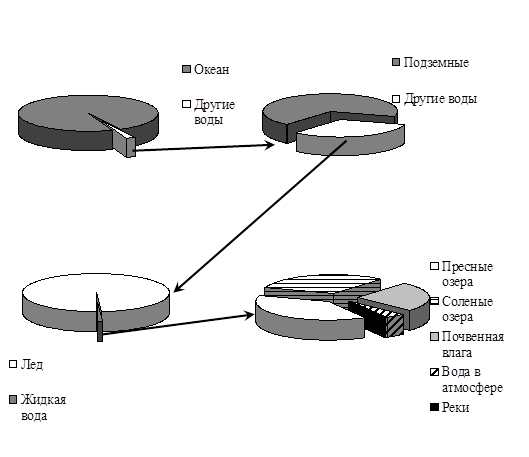
Рис. 16. Состав гидросферы по
классам вод.
Таблица 4
Средний состав речных вод (мг л-1)
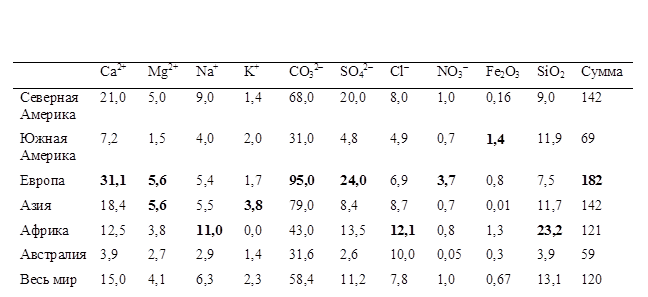
|

