|
О.А. Федяева
Промышленная экология
Конспект лекций. – Омск: Изд-во ОмГТУ, 2007. - 145 c.
Глава 2. Защита атмосферы
2.4. Очистка отходящих газов от оксидов азота
2.4.1. Абсорбционные методы
Для абсорбции оксидов азота используют воду, растворы
щелочей, селективные сорбенты, кислоты и окислители.
При абсорбции NO2 водой в газовую фазу выделяется часть оксида азота,
скорость его окисления при низких температурах мала:
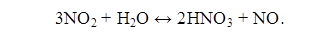
Для утилизации оксидов можно использовать разбавленные
растворы H2O2 с получением
азотной кислоты:
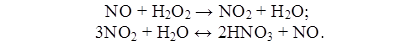
При этом расходуется 6 кг H2O2 на 1 т кислоты в сутки.
Хемосорбция NO2 раствором соды протекает по уравнению:
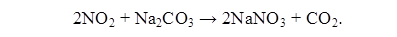
При абсорбции растворами аммиака образуются соединения
с низкой температурой разложения. Например, нитрат аммония NH4NO2 при 56 оС полностью распадается:
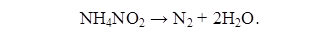
Для очистки газов от NO при
отсутствии в газовой фазе кислорода, могут быть использованы растворы FeSO4, FeCl2, Na2S2O3, NaHCO3. При этом для первых двух
растворов протекают реакции с образованием комплексов:
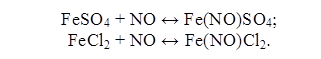
При нагреве до 95-100 оС комплекс Fe(NO)SO4 распадается и NO выделяется в
чистом виде, а восстановленный раствор вновь возвращается в производство.
Аналогично разлагается комплекс Fe(NO)Cl2.
Использование растворов Na2S2O3, NaHSO4, (NH2)2CO приводит к дефиксации азота:
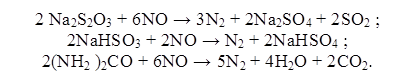
При температуре выше 200 оС NO
взаимодействует с аммиаком:
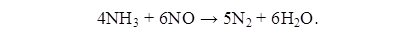
Серная кислота используется для
поглощения NO2 и N2O3 с образованием нитрозилсерной кислоты:
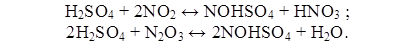
При нагревании нитрозилсерной кислоты или при
разбавлении её водой происходит выделение оксидов азота:
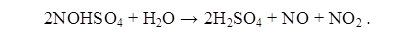
Взаимодействие оксидов азота с жидкими сорбентами
наиболее эффективно при 20-40 оС.
|

